シロシビンという名前を聞いて、どんなイメージを持つだろうか。
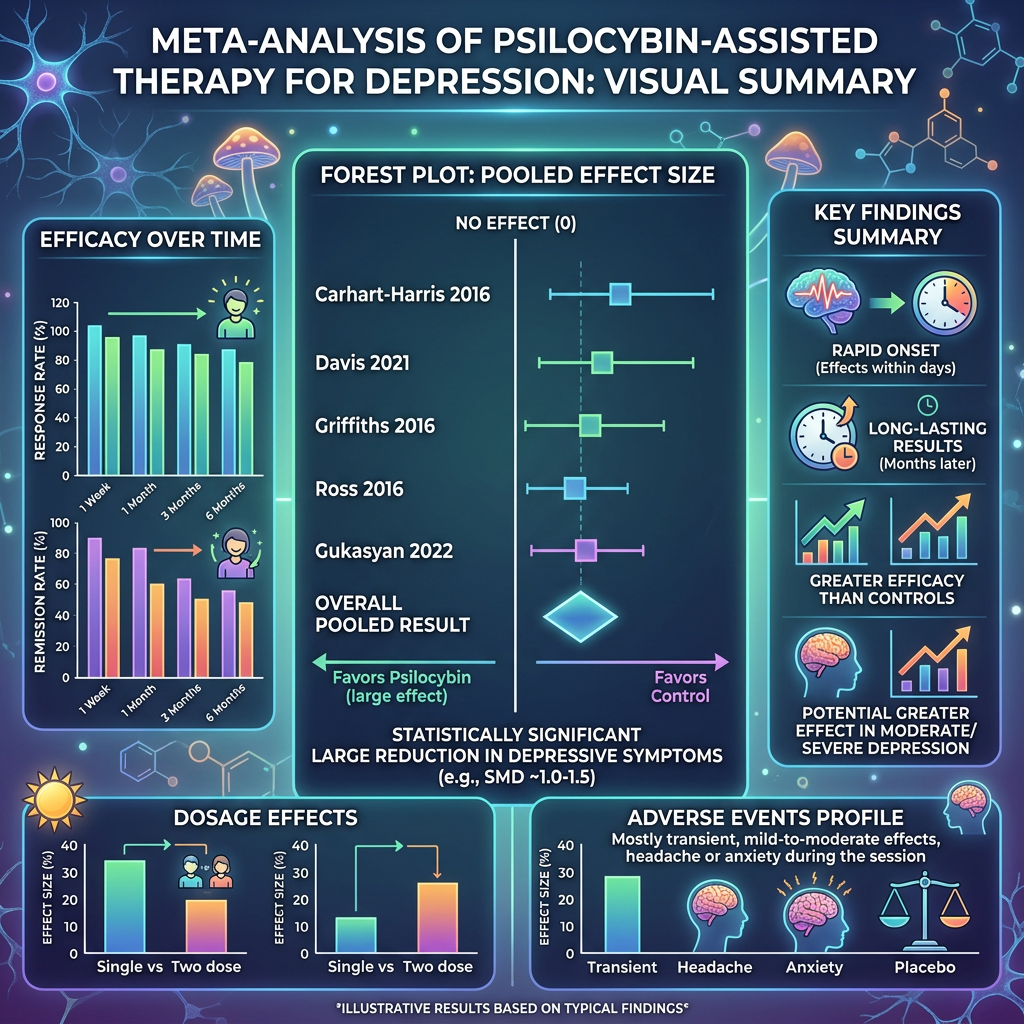
いわゆる「マジックマッシュルーム」に含まれる化合物として知られるシロシビンが、今や精神医学の最前線で真剣に研究されています。Singleton らが Nature Mental Health に発表した研究は、このシロシビンのうつ病治療効果について、15の無作為化比較試験を統合したメタ解析の結果を報告しました。
「リビングシステマティックレビュー」という新しいアプローチが、この研究の特徴の一つです。
従来の系統的レビューは、ある時点でのデータを集めて分析し、そこで完結しますが、リビングシステマティックレビューでは、新しい研究結果が出るたびに継続的にデータを更新し続ける仕組みになっています。
これは現代の医学研究において画期的なことです。特にシロシビンのような新しい可能性のある治療法では、日々新しい臨床試験の結果が報告されます。その都度、エビデンス全体を見直し、最新の知見を反映できるのは大きなメリットでしょう。
シロシビンがうつ症状を軽減する可能性が、この統合解析から見えてきました。
シロシビンの作用機序は従来の抗うつ薬とは根本的に異なります。セロトニン2A受容体に作用し、一時的に意識状態を変化させることで、脳の神経回路の柔軟性を高めるとされています。いわば「脳のリセット」のような効果が期待されているのです。
まだ多くの人にとって受け入れがたいかもしれません。
最初にシロシビンの研究を知った時は少し驚きました。しかし、医学の歴史を振り返ると、天然由来の化合物が重要な治療薬になった例は数知れません。アスピリン、メトホルミン、モルヒネ、ジギタリス、SGLT2阻害薬—どれも植物由来の成分から開発されました。
シロシビンも同様に、適切にコントロールされた医療環境下では、新たな治療選択肢になる可能性があります。特に既存の抗うつ薬に反応しない患者にとって、希望の光になるかもしれないのです。
オープンデータ・リソースとして研究結果を公開している点も評価したいと思います。
科学の進歩は、Open Science(データの透明性と共有)によってもたらされます。この研究チームが生データを公開することで、他の研究者が独自の解析を行ったり、新しい仮説を検証したりもできます。
精神医学の分野では、研究の再現性や透明性が重要な課題となっています。Open Scienceの実践は、この分野の信頼性向上にも寄与することでしょう。
一方、臨床応用への道のりは、まだ険しいものがあります。
シロシビン治療には、専門的な訓練を受けた医療スタッフによる厳重な監視が必要です。投与中の患者は数時間にわたって特殊な精神状態を経験するため、適切なサポート体制が不可欠です。
また、すべてのうつ病患者に適応があるわけではありません。精神病の既往歴がある患者や、特定の心疾患を持つ患者には禁忌です。
規制の観点からも課題は多いです。現在、シロシビンは多くの国で規制薬物として分類されています。医療用途での使用を認めるには、法的枠組みの整備が必須です。
既存の治療法では十分な効果が得られない患者さんはたくさんいらっしゃいます。精神的な不調が原因不明の身体症状として現れる患者さんも少なくありません。
科学的根拠に基づいた安全で効果的な治療法である限り、新しい治療選択肢が増えることは、医療者にとっても患者にとっても歓迎すべきことです。
このリビングシステマティックレビューが今後どのように発展し、どんな新しい知見を提供してくれるのか。そして、シロシビン治療が本当に精神医学の新たな標準治療となり得るのか。その答えを、リアルタイムで見届けることになるのかもしれません。
(論文はコチラから読めます)